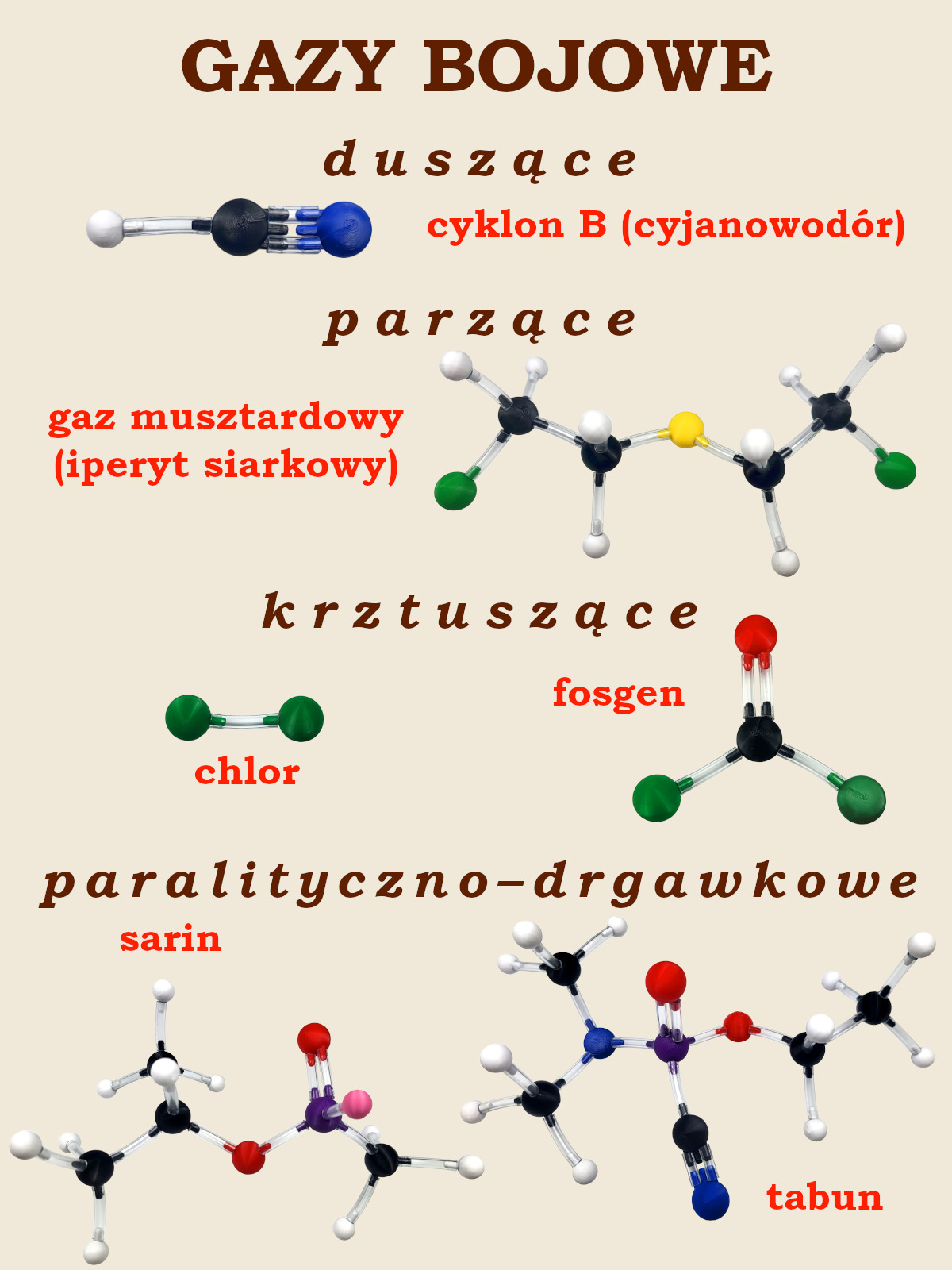
Gazy bojowe – przegląd
cyklon B, iperyt, chlor, fosgen, sarin i tabun
Różne są drogi prowadzące do zainteresowania chemią. W niektórych przypadkach u źródła leży dziecięca fascynacja wybuchami lub zastosowaniami militarnymi. Wychodząc naprzeciw tej właśnie grupie młodych adeptów chemii, opowiemy dzisiaj o najpopularniejszych gazach bojowych. 😊
Wszystkie omówione dzisiaj cząsteczki możesz ułożyć mając 200‑elementowe (rozszerzone) zestawy „Atomków” do chemii nieorganicznej i chemii organicznej.
Informacje wstępne
Różnego rodzaju chemicznych środków bojowych w postaci zatrutych strzał lub śmierdzących oparów używano już od starożytności. Jednak na powszechną skalę zaczęto ich używać dopiero w I Wojnie Światowej. Na początku były to głównie gazy łzawiące o dosyć niskiej skuteczności, jednak z czasem zaczęto używać bardziej śmiercionośnych substancji.
W późniejszych czasach wiele międzynarodowych konwencji zabraniało posiadania i używania broni chemicznej. Niestety, wbrew tym umowom, zapasy tej broni w arsenałach armii całego świata ciągle rosły i jest ona (na szczęście: sporadycznie) używana aż do dziś.
Choć przez ostatni wiek postępy w wymyślaniu nowych trucizn są ogromne, to wiele z gazów używanych w czasie I Wojny Światowej jest stosowanych nadal ze względu na ich prostotę, skuteczność i łatwość produkcji.
Poznamy dzisiaj te najpopularniejsze w podziale stosowanym przez wojskowych.
🧪 Duszące gazy bojowe 🧪
Do tej grupy należą przede wszystkim substancje będące źródłem jonu cyjankowego (CN–). Jon ten jest izoelektronowy (to mądre określenie na identyczną konfigurację elektronową tych drobin) z cząsteczką trującego tlenku węgla(II) (czadu), więc zachowuje się podobnie jak ona. Wiąże żelazo w hemie tworząc kompleks trwalszy niż żelazo tworzy z cząsteczkami tlenu. Blokuje to transport tlenu z płuc do tkanek powodując ich obumieranie (uduszenie).
Najprostszym ale bardzo skutecznym przedstawicielem tej grupy jest cyklon B, czyli ziemia okrzemkowa nasycona cyjanowodorem. Cyjanowodór nie był powszechnie stosowany na polach bitewnych, natomiast służył Niemcom do uśmiercania ludzi w komorach gazowych w niemieckich obozach zagłady.

🧪 Parzące gazy bojowe 🧪
Środki te powodują poparzenia skóry. Często nie są śmiertelne, jednak nie da się przed nimi ochronić za pomocą maski przeciwgazowej, więc powodują chaos w szeregach zaatakowanych oddziałów i konieczność udzielania pomocy jednocześnie bardzo wielu rannym.
Najpopularniejszym ich przedstawicielem jest iperyt siarkowy, który z chemicznego punktu widzenia jest tioeterem (czyli eterem z atomem siarki zamiast atomu tlenu).
W postaci czystej jest to ciecz o bardzo słabym zapachu. Jednak stosowany jako broń iperyt techniczny ma silny zapach musztardy, stąd alternatywna nazwa tej substancji: gaz musztardowy.
Po II Wojnie Światowej duża część niemieckich zapasów iperytu została zatopiona przez aliantów w Morzu Bałtyckim. Swoje dołożyli też Rosjanie, którzy jeszcze w latach 90‑tych pozbywali się w ten sposób starych zapasów ze swoich baz na Łotwie i w Estonii. Na dnie morza, w warunkach niskiej temperatury i podwyższonego ciśnienia iperyt uległ zestaleniu. Wyciagane w sieciach rybackich lub wyrzucane na brzeg morza kawałki iperytu były wielokrotnie przyczyną poparzeń rybaków i turystów. Na przykład, w 1955 w Darłówku poparzeniu uległo 102 dzieci będących tam na koloniach, z czego czwórka trwale straciła wzrok.
Nazwa iperytu pochodzi od miejscowości Ypres w Belgii, gdzie ta substancja została po raz pierwszy użyta w warunkach bojowych.

🧪 Krztuszące gazy bojowe 🧪
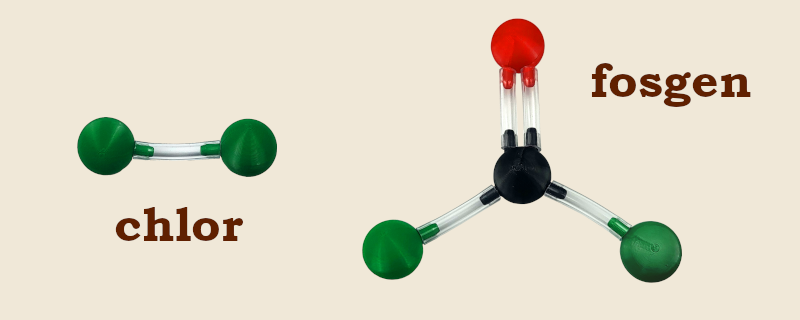
Celem użycia tych gazów nie jest bezpośrednie zadanie strat przeciwnikowi, ale doprowadzenie żołnierzy do kaszlu i wymiotów, co uniemożliwi im założenie masek przeciwgazowych, przez co będą narażeni na atak innymi środkami chemicznymi. Najpopularniejszymi przedstawicielami tej grupy gazów bojowych są chlor i fosgen.
Chlor jest środkiem tanim w produkcji i niestety skutecznym w działaniu. Silnie podrażnia drogi oddechowe, jednocześnie przy bezwietrznej pogodzie długo pozostając przy powierzchni ziemi, gdyż jest gazem znacznie cięższym od powietrza. Po raz pierwszy został użyty w czasie I Wojny Światowej, kiedy wykazał się śmiertelną skutecznością. Na przykład, 31 maja 1915 Niemcy rozpylili 264 tony chloru pod Bolimowem (miejscowość leżąca w okolicach Łowicza i Skierniewic), w wyniku czego zginęło 1183 żołnierzy, a prawie 10 tysięcy uległo zatruciu.
Jednak częściej w tej roli stosuje się fosgen. Z chemicznego punktu widzenia fosgen to chlorek kwasu węglowego. W tym miejscu zachęcam, aby przeczytać nasz wcześniejszy artykuł o chlorkach kwasowych.
Fosgen to bezbarwny gaz o zapachu zgniłych owoców. Jego działanie jest gorsze niż chloru, bo nie wywołuje on kaszlu, co powoduje napełnienie się płuc płynem. Takie zdradliwe działanie fosgenu może spowodować śmierć osoby nie zdradzającej objawów zatrucia nawet po 48 godzinach od ataku. Był to jeden z najczęściej używanych gazów bojowych w czasie I Wojny Światowej.
🧪 Paralityczno‑drgawkowe gazy bojowe 🧪
Działanie tych środków ma dosyć skomplikowany mechanizm. W dużym skrócie polega ono na trwałym związaniu enzymu (acetylocholinoesterazy), który jest odpowiedzialny za szybki rozkład neuroprzekaźnika (acetylocholiny) odpowiedzialnego za skurcz mięśni. W wyniku tego następuje przesycenie synaps i utrata kontroli mózgu nad mięśniami. Objawy zatrucia następują stopniowo i prowadzą do porażenia mięśni, śpiączki i śmierci w wyniku uduszenia się lub zatrzymania akcji serca.
Wszystkie substancje z tej grupy mają podobną budowę chemiczną – są organicznymi pochodnymi kwasu fosfonowego (czyli fosfonianami) lub fosforowego (czyli fosforanami). Wybraliśmy dla Was dwa najpopularniejsze gazy bojowe – sarin i tabun. Ich cząsteczki omówimy dokładniej, bo będzie to okazja aby poznać wiele struktur, o których nigdy nie wspomina się w szkole.
Sarin
Zacznijmy od kwasu fosfonowego. Uważni czytelnicy bloga pamiętają na pewno nasz artykuł o kwasie ortofosforowym(III) i jego formie H‑fosfonianowej. Kwas fosfonowy, to po prostu inna nazwa kwasu ortofosforowego(III), nadana tak ze względu na jego dominującą formę tautomeryczną. To własnie tą nazwą posługują się najczęściej chemicy organicy i dlatego pochodne tego kwasu zostały nazwane fosfonianami.
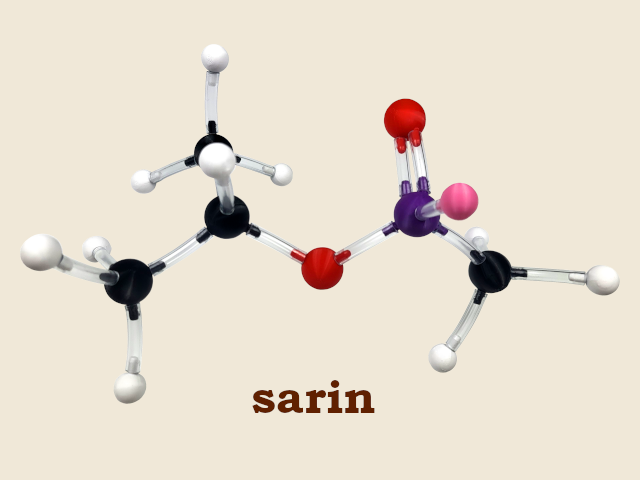
Popatrzmy na cząsteczkę sarinu wychodząc właśnie od kwasu fosfonowego. Po prawej stronie widać wiązanie P—C tak charakterystyczne dla fosfonianów. Grupa metylowa podstawiona została w miejsce atomu wodoru w cząsteczce kwasu. Jeżeli atom wodoru by pozostał w tym miejscu, to mówilibyśmy, że związek ten należy do tzw. H‑fosfonianów.
Kolejne wiązanie od atomu fosforu prowadzi do atomu fluoru podstawionego w miejsce grupy —OH. Możemy zatem powiedzieć, że związek ten jest w tej części fluorkiem kwasowym. Fluorki kwasowe, to związki analogiczne do wspomnianych wcześniej chlorków kwasowych. W tej sytuacji nie będzie już dla ucznia zdziwieniem, że istnieją też bromki kwasowe i jodki kwasowe.
Teraz patrzymy na lewą część cząsteczki, gdzie za pośrednictwem atomu tlenu podłączony jest łańcuch trzech atomów węgla. To, oczywiście, jest grupa estrowa. Kwas ortofosforowy(III) korzystając z drugiej ze swoich grup hydroksylowych (przypominamy, że kwas fosforowy(III) jest kwasem dwuprotonowym) utworzył ester z propan‑2‑olem.
Czyli, podsumowując, sarin to związek z grupy fosfonianów, który jest też jednocześnie fluorkiem kwasowym i estrem. Prawda, że teraz ta cząsteczka wydaje się dużo mniej tajemnicza? 😀
Tabun
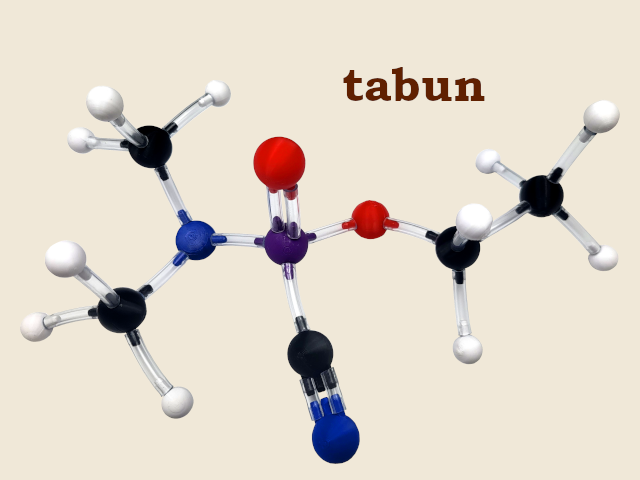
Omówmy teraz cząsteczkę tabunu. Tabun jest pochodną świetnie nam znanego kwasu ortofosforowego(V). Na wstępie odnajdźmy elementy znajome. Widać skierowaną w prawo grupę estrową. Tak – tabun też jest estrem! W tej części cząsteczki jest to ester kwasu ortofosforowego(V) oraz dobrze uczniom znanego etanolu.
Po lewej stronie cząsteczki widzimy dwie grupy metylowe podłączone do atomu fosforu za pośrednictwem atomu azotu. Otóż, tak jak możemy zamienić grupę –OH tlenowego kwasu nieorganicznego lub kaboksylowego podstawiając w to miejsce atom halogenu i otrzymując odpowiedni halogenek kwasowy, tak analogicznie możemy podstawić w miejsce grupy –OH grupę –NH2 otrzymując tzw. amid kwasowy. Jeżeli będziemy zamieniać atomy wodoru w tej grupie na łańcuchy organiczne, to otrzymamy kolejno amidy pierwszo- i drugorzędowe. Popatrzmy teraz na cząsteczkę tabunu i zauważmy, że do atomu azotu podłączone są dwie grupy metylowe, więc tabun w tej części jest dimetyloamidem kwasu ortofosforowego(V).
Został nam ostatni fragment cząsteczki zawierający nieznaną uczniom grupę –CN podłączoną bezpośrednio do atomu fosforu. Jest to tzw. grupa nitrylowa. Związki posiadające taką grupę to nitryle. Najprostszy nitryl (CH3—CN) znany pod nazwą acetonitryl lub cyjanometan, to często spotykany w laboratorium organicznym rozpuszczalnik. Większość związków nitrylowych jest szkodliwa dla zdrowia, czego omawiany tabun jest świetnym przykładem.
W naszej cząsteczce grupa —CN podłączona jest zamiast grupy —OH do atomu fosforu. Otrzymujemy w ten sposób dosyć rzadką strukturę cyjanidu kwasowego. Jest to struktura analogiczna do halogenku kwasowego lub amidu kwasowego, w której grupę —OH zastępuje inna grupa. Jednak zapamiętać należy, że zamiana na grupę —CN możliwa jest tylko w nieorganicznych kwasach tlenowych. W kwasach karboksylowych próba przyłączenia grupy cyjankowej spowoduje powstanie tzw. cyjanohydryn z powodu niemożności istnienia obok siebie grupy nitrylowej (—CN) i karbonylowej (>C=O).
Patrząc teraz na cząsteczkę tabunu pownniśmy widzieć cząsteczkę znanego nam ze szkoły kwasu ortofosforowego(V), w której jedna grupa hydroksylowa została zestrowana etanolem, druga grupa podstawiona grupą dimetyloamidową, a trzecia grupą nitrylową. Struktura ta jest więc o wiele prostsza niż wygląda na pierwszy rzut oka.
Aby swobodnie układać cząsteczki gazów bojowych warto zaopatrzyć się w zestawy rozszerzone (200‑elementowe) do chemii nieorganicznej i chemii organicznej.
Koniecznie polub też profil „Atomków” i dodaj go do ulubionych, aby nie przegapić kolejnych ciekawych wpisów. 👨🔬
Łukasz Aranowski
13 października 2024